Más Información

Primer Simulacro Nacional 2026: este será el mensaje de alerta que llegará a los celulares; evita que te tome por sorpresa

Día de la Santa Cruz 2026; la mejor mezcla de frases y memes para celebrar a los albañiles este 3 de mayo
La comunidad científica recibió con gran entusiasmo las buenas noticias sobre la vacuna contra el coronavirus desarrollada por las compañías farmacéuticas Pfizer y BioNTech: un 95% de efectividad, ningún efecto secundario preocupante y buena protección para personas mayores de 65 años y de diferentes razas y etnias.
La efectividad se midió utilizando a los 170 voluntarios de los ensayos clínicos de Fase III que fueron diagnosticados con covid-19, pues al comparar los resultados los científicos constataron que la gran mayoría de participantes infectados pertenecían al grupo al que se le había administrado un placebo, es decir, una sustancia sin efecto terapéutico.
Esto significa que la gran mayoría de voluntarios inmunizados parecen haber sido protegidos del Sars-CoV-2, el coronavirus responsable de la pandemia.
Y aunque el estudio, en el que participan más de 43.000 personas repartidas por Sudáfrica, Alemania, Argentina, Brasil, Estados Unidos y Turquía, continuará durante varios meses, estos hallazgos preliminares servirán para que Pfizer y BioNTech soliciten una autorización de emergencia para su producto a la FDA, la agencia reguladora de los Estados Unidos, "en los próximos días".
La de Pfizer y BioNTech no es la única candidata al borde de la aprobación.
En un comunicado difundido el 16 de noviembre, el laboratorio Moderna informó que su inmunizador había registrado una tasa de efectividad del 94%.
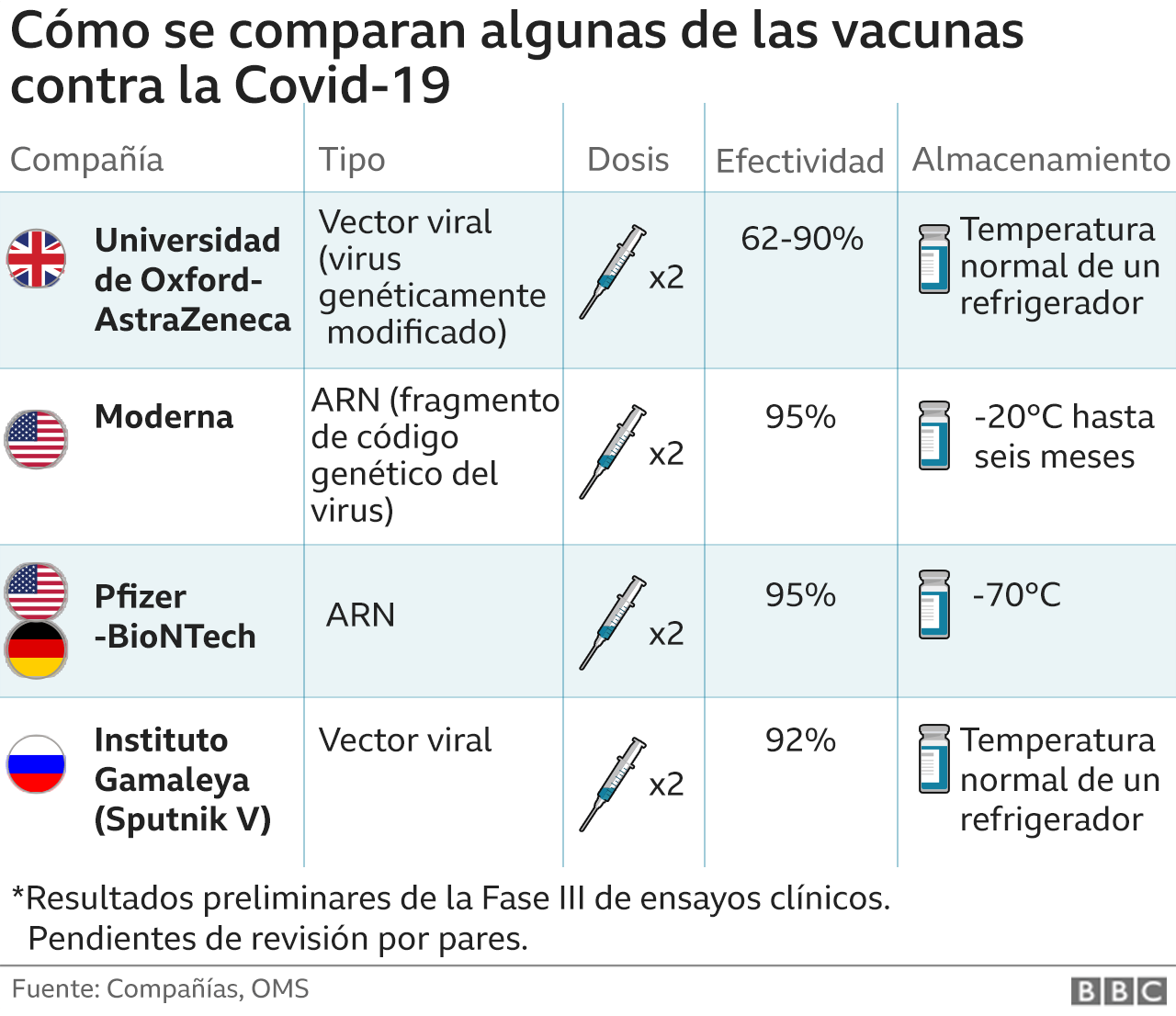
Y esta semana se dieron a conocer los resultados preliminares de la vacuna desarrollada por la Universidad de Oxford y AstraZeneca, que muestran que es un 70,4% efectiva.
Pero, ¿cuáles son las fortalezas y debilidades de cada competidor en esta carrera por una vacuna? Ha llegado el momento de conocerlos.
1. BNT162 (Pfizer y BioNTech)
Por lo que se sabe hasta el momento, la vacuna BNT162 es una de las más avanzadas y debería ser aprobada por Estados Unidos en las próximas semanas.
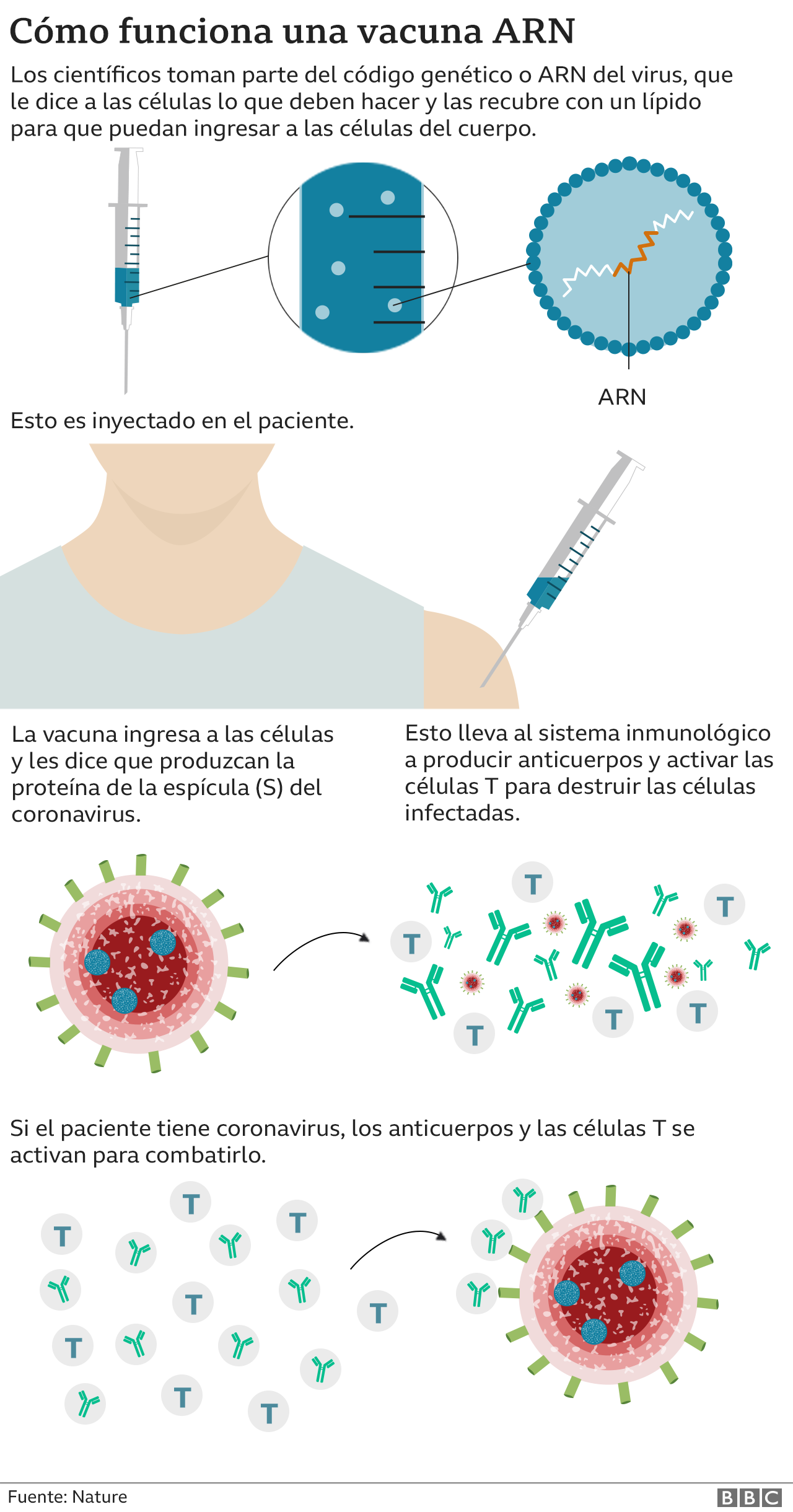
Esta utiliza la tecnología conocida como ARN: es decir, contiene una pequeña secuencia genética creada en el laboratorio que "enseña" a las propias células del cuerpo humano a producir proteínas similares a Sars-CoV-2. A partir de ahí, el sistema inmunológico reconoce la amenaza y crea una respuesta que protege al cuerpo de futuras infecciones.
Cabe destacar que los resultados anunciados por Pfizer y BioNTech aún necesitan ser publicados en alguna revista científica y evaluados por expertos independientes.
Pero si son consistentes, representarán un cambio de paradigma en la ciencia, pues la suya sería la primera vacuna genética de la historia.
¿Cuál es la ventaja de esto? Primero, son mucho más fáciles y rápidas de producir. Luego, los requisitos de laboratorio y equipo son menores en comparación con los inmunizadores que tenemos hasta ahora.
Pero el mayor inconveniente es la necesidad de mantener las dosis a una temperatura inferior a -70° C para evitar que la sustancia pierda su efecto. Esto puede convertirse en un obstáculo importante en regiones remotas o muy cálidas.
En entrevistas recientes, los representantes de Pfizer dijeron que están pensando en soluciones y tecnologías para garantizar una temperatura tan baja, menor incluso que el más frío invierno en la Antártida.
Otro problema sería la disponibilidad de este inmunizador en los países en desarrollo.
Por ahora, por ejemplo, y a pesar de la participación de Brasil en las pruebas, no existe ningún arreglo para la compra o transferencia de tecnología al país. E incluso si el gobierno brasileño y las dos empresas cierran un acuerdo, las primeras dosis solo llegarían a Brasil a partir del primer trimestre de 2021, pues otras naciones ya se han garantizado los primeros lotes.
2. mRNA-1273 (Moderna)
Esta candidata también forma parte del grupo de vacunas basadas en ARN. El reciente anuncio de Moderna, por su parte, se basó en 95 participantes en ensayos clínicos diagnosticados con covid-19. Los resultados muestran que 90 de ellos eran del grupo placebo, lo que sugiere una tasa de efectividad del 94%.
También hay otras buenas noticias relacionadas con esta primer informe: el inmunizador no causó ningún evento adverso notable y generó una respuesta constante del sistema inmunológico incluso en los ancianos o en personas con enfermedades crónicas. También parece prevenir casos graves que requieren hospitalización e intubación.
Antes de solicitar la aprobación, sin embargo, el fabricante de medicamentos debe esperar un poco más para completar el objetivo de 150 eventos (es decir, 150 participantes infectados de covid-19) para tener datos más sólidos. Esto debería suceder en las próximas semanas.
Comparado con el competidor Pfizer y BioNTech, el producto de Moderna tiene la ventaja de almacenarse a menos de 20° C. Esta es una temperatura mucho más fácil de garantizar con los congeladores que tenemos actualmente.
No hay mucha información sobre la posible llegada de esta vacuna a los países en desarrollo. Una forma de obtener el producto puede ser el Fondo Global de Acceso a Vacunas para Covid-19 (Covax), creado por la Organización Mundial de la Salud con el objetivo de distribuir dosis a países menos desarrollados. Numerosos países latinoamericanos son parte de esta iniciativa.
3. AZD1222 (Universidad de Oxford y AstraZeneca)
También probada en Brasil, esta candidata pertenece al equipo de vacunas de vectores virales no replicantes.
Esto quiere decir que se construyó a partir de un adenovirus, un tipo de virus que no daña nuestra salud. En su interior, los científicos insertaron algunos genes de Sars-CoV-2 para provocar una reacción del sistema inmunológico.
A la vacuna le ha ido bien en ensayos clínicos: la información completa del estudio de Fase II se publicó el 19 de noviembre en The Lancet y confirmó que el inmunizador es seguro y no causa efectos secundarios graves, incluso en ancianos. Otro punto a destacar es que produjo anticuerpos, una gran señal.
El 23 de noviembre, los desarrolladores de la vacuna divulgaron los resultados preliminares de la Fase III de ensayos clínicos.
De acuerdo al análisis de 131 casos de covid-19, esta vacuna demostró ser un 70,4% efectiva al combinar datos obtenidos de un régimen de dos dosis administradas. Los investigadores estiman, sin embargo, que dicha eficacia pueda llegar al 90% si se ajusta la dosis.
Las fortalezas y debilidades de AZD1222 están en su originalidad: hasta el momento, no existe una vacuna aprobada que utilice este tipo de metodología. Por un lado, esto puede funcionar y revolucionar el conocimiento en el campo. Por otro, es necesario esperar pacientemente los resultados definitivos sobre la efectividad y seguridad del producto.
Una ventaja de la vacuna de la Universidad de Oxford y AstraZeneca está en su disponibilidad. Entre otros, Brasil, Argentina y México ya tienen convenios para la compra y transferencia de tecnología.
A nivel mundial, los responsables de esta vacuna garantizan que tendrán capacidad para entregar 3.000 millones de unidades en 2021.
Otra ventaja de este compuesto es que puede guardarse a una temperatura de entre 2 y 8 °C, por lo cual puede distribuirse y preservarse con capacidades logísticas existentes.
4. CoronaVac (Sinovac)
Esta vacuna china copó titulares la semana pasada, luego de la suspensión de las pruebas clínicas en Brasil por la muerte de un voluntario. La Agencia Nacional de Vigilancia Sanitaria (Anvisa) y el Instituto Butantan intercambiaron críticas en una serie de notas y entrevistas colectivas.
Pero pocos días después se aclaró que la muerte no había tenido nada que ver con la vacuna y se retomó el estudio con normalidad.
Dejando a un lado la polémica, la farmacéutica Sinovac también apuesta por la estrategia del virus inactivado. Los científicos utilizaron algún método, como calor o productos químicos, para desactivar el Sars-CoV-2 y que no cause infección ni se reproduzca dentro del cuerpo. Aun así, cuando se aplica en una vacuna, el virus es reconocido por el sistema inmunológico, creando una respuesta protectora.
El punto fuerte aquí es la fiabilidad. La ciencia ha estado trabajando con vacunas de virus inactivados durante casi siete décadas. Por eso ya sabemos muy bien cómo producirlas y los principales problemas que pueden aparecer por el camino.
En la dirección opuesta, el punto débil es el retraso. La fabricación requiere un rigor extremadamente alto y una planta industrial muy bien equipada. La formulación tampoco rinde mucho en dosis por litro.
El producto se encuentra en la Fase III de prueba y pronto espera completar la cantidad mínima de eventos (voluntarios infectados con covid-19) para calcular su tasa de efectividad, como sucedió recientemente con Pfizer / BioNTech y Moderna.
La refrigeración no parece ser un problema, ya que otras vacunas de virus inactivados pueden guardarse en un refrigerador convencional.
Otro punto positivo es el acuerdo entre Sinovac y el Instituto Butantan, en São Paulo, que debería facilitar el acceso a CoronaVac en Brasil y América Latina.
5. Sputnik V (Centro Gamalaya de Investigación en Epidemiología y Microbiología)
Durante mucho tiempo, la palabra que mejor definió a la vacuna Sputnik V fue misterio. Las primeras noticias de Rusia, donde se encuentra el Instituto de Investigación Gamalaya, decían que ya se encontraba en una etapa avanzada de investigación. Poco después, fue aprobada por el gobierno.
Los especialistas estaban muy preocupados porque las pruebas clínicas que garantizan la confiabilidad del proceso de investigación no habían sido registradas ni publicadas en ninguna revista científica.
Desde entonces, ha surgido mucha información: la vacuna se basa en el vector viral no replicante (del mismo tipo en la Universidad de Oxford / AstraZeneca) y se está probando en unos 40.000 voluntarios en países como Rusia, Emiratos Árabes Unidos, Venezuela y Bielorrusia.
Con base en uno de estos análisis preliminares, los investigadores de la Sputnik V anunciaron una efectividad del 92%, basándose en 20 eventos registrados. Hay que esperar a que el estudio evolucione un poco más para que este ritmo se consolide.
Se especula que el inmunizador no requiere congelación, pero esa información aún no se ha confirmado.
6. JNJ-78436735 (Johnson & Johnson)
Sudáfrica, Argentina, Brasil, Chile, Colombia, Estados Unidos, México y Perú son los países donde actualmente se prueba la vacuna de Johnson & Johnson. Hay más de 60 mil voluntarios en estos países.
Basada en la tecnología del vector viral no replicante (el mismo utilizado por la Universidad de Oxford / AstraZeneca y la Sputnik V), parece estar un poco retrasada, ya que la farmacéutica no ha hecho anuncios de análisis preliminares. Se espera que suceda en las próximas semanas.
La principal ventaja estaría en los números: parte de los estudios de Fase III evalúa una sola aplicación de la vacuna. Los otros competidores necesitan dos dosis para tener efecto. Si este esquema funciona, podría significar ahorros de miles de millones de dólares.
7. NVX-CoV2373 (Novavax)
Este es el representante más avanzado de la clase de vacunas de subunidades de proteínas. En lugar de utilizar todo el virus, se desarrolló a partir de un pequeño fragmento de Sars-CoV-2 capaz de activar una respuesta inmunitaria.
En relación con los competidores enumerados anteriormente, el desempeño de Novavax tardará más en conocerse. Parte de los estudios de Fase III se llevan a cabo en el Reino Unido con 15.000 voluntarios y se esperan resultados preliminares en enero o febrero de 2021.
Hay otra parte de esta investigación que se realizará con decenas de miles de participantes en Estados Unidos. Se espera que la etapa comience a fines de noviembre o principios de diciembre.
Como el producto de Novavax es parte de Covax (ese consorcio de la OMS para la compra y distribución de dosis a países menos desarrollados), es posible que llegue a América Latina en algún momento, si todo va bien.
8. Ad5-nCoV (CanSino)
También elaborada a partir de un vector viral que no se replica (como los candidatos de la Universidad de Oxford / AstraZeneca, Sputnik V y Johnson & Johnson), fue aprobada de emergencia para su uso por personal militar chino, incluso antes de importantes estudios de seguridad y eficacia.
En las pruebas de Fase III, la Ad5-nCoV se aplica actualmente a más de 40.000 voluntarios de Pakistán, Arabia Saudita y México.
Hay poca información sobre esta vacuna así que es necesario esperar nuevos anuncios por parte de los responsables.
9. Covaxin (Bharat Biotech)
Desarrollada en India, es una de las últimas candidatas en entrar en la Fase III de ensayos clínicos. Al igual que CoronaVac, también utiliza virus inactivados en su formulación.
Como se mencionó anteriormente, existe una gran experiencia mundial en el uso de esta tecnología, aunque es costosa y requiere mucho tiempo en comparación con los métodos más modernos.
Para los ensayos, los responsables pretenden reclutar a más de 25.000 participantes en territorio indio. Según un informe de Reuters, se espera que la distribución de dosis comience a partir de febrero de 2021.
Pronto se darán a conocer más detalles sobre Covaxin.
Ahora puedes recibir notificaciones de BBC News Mundo. Descarga nuestra app y actívalas para no perderte nuestro mejor contenido.
Noticias según tus intereses
[Publicidad]
[Publicidad]